導讀
高效、綠色、廉價的反應體系一直是化學家們在過渡金屬催化不對稱氫化領域內的不懈追求。近日,上海交通大學張萬斌教授課題組報道了一種豐產金屬鎳催化α-取代丙烯酸的不對稱氫化反應,高效地合成了一系列手性α-取代丙酸衍生物。反應取得了最高99.4%的對映選擇性和10000的催化轉化數。特別是在不對稱催化氫化青蒿酸的克級規模反應中,以5000的轉化數得到抗瘧疾藥物青蒿素的關鍵中間體二氫青蒿酸。該催化體系的發展對豐產金屬鎳催化不對稱氫化工業化的套用具有積極的作用。相關成果發表在
Nature Communications
上( https://doi.org/10.1038/s41467-024-49801-0 )。正文
手性α-取代丙酸是一類非常重要的化合物,其結構廣泛存在於生物活性化合物和有機中間體中(圖1a)。手性α-芳基取代丙酸類衍生物,如(
S
)-布洛芬、(S
)-萘普生、(S
)-氟比洛芬和(S
)-酮洛芬等,在人體內具有抑制前列腺素合成的作用,是一類非常重要的抗炎和鎮痛藥物。此外,世界著名的抗瘧疾藥物青蒿素和廣泛使用的手性中間體(S
)-羅氏酯則屬於手性α-烷基取代丙酸衍生物。鑒於這些化合物的重要性,它們的不對稱合成一直是化學家們研究的一個重要課題。相比於其他不對稱合成方法,過渡金屬催化的不對稱氫化具有高效性且易於工業化生產的優點,被廣泛套用於這類化合物的合成研究中。然而目前該領域主要集中於使用稀有金屬催化劑,對於豐產金屬催化劑涉及較少,效果有待提高。近年來,豐產金屬催化劑(如錳、鐵、鈷、鎳、銅)在不對稱催化氫化研究中取得了重大的進展,他們具有價格低廉,毒性很低等優點,符合綠色化學的要求。然而,由於二取代烯烴的空間位阻較低,使得反應中立體選擇性難以控制,目前大多數研究主要集中在三取代烯烴和四取代烯烴的不對稱氫化上。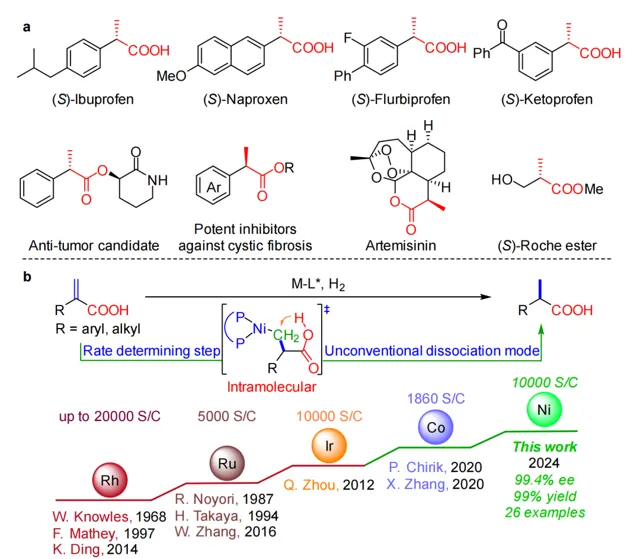
圖1 重要手性α-取代丙酸衍生物以及其不對稱氫化合成策略
上海交通大學張萬斌教授團隊近年來一直致力於過渡金屬催化的不對稱氫化研究,並行現了一些反應中存在著催化劑與受質之間CHHC弱吸引交互作用,也稱為多重色散交互作用(MADI),這種交互作用協同參與了反應過程,顯著地提高了反應的活性和對映選擇性(Pd:
Angew. Chem. Int. Ed.
201352
, 11632;201655
, 8444;Nature Commun.
9
, 5000;iScience
202023
, 100960; Rh:201958
, 11505)。在此基礎上,他們進一步開發了一系列豐產金屬(鎳、鈷、銅)參與的不對稱催化氫化反應(201958
, 7329;201958
, 15767;202059
, 5371;Nat. Commun.
202011
, 5935;202160
, 16989;Nat. Chem.
202214
, 920;202362
, e202214990;202362
, e202217871;202362
, e202303488; 等)。近日,他們將其套用於二取代烯烴的不對稱氫化研究中,報道了一種高效的鎳催化α-取代丙烯酸的不對稱氫化反應,以高達99.4%的對映選擇性得到相應的手性α-取代丙酸衍生物,反應轉化數可達10000(圖1b)。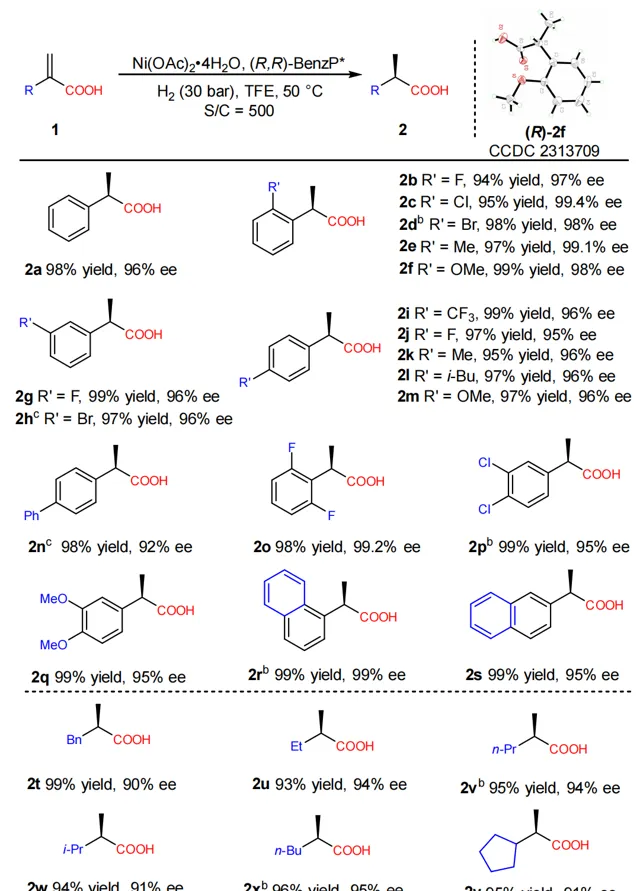
圖2 受質適用性研究
作者在獲得最優反應條件後,對反應受質適用性進行了探索。大部份受質都能在轉化數為500條件下以優秀的收率(93-99%)和對映選擇性(90-99.4%)得到相應產物。該反應體系能很好的適用於鄰位,間位,對位取代的單取代,多取代,以及聯苯基,萘環,鏈烷基,環烷基礎類別的受質(圖2)。
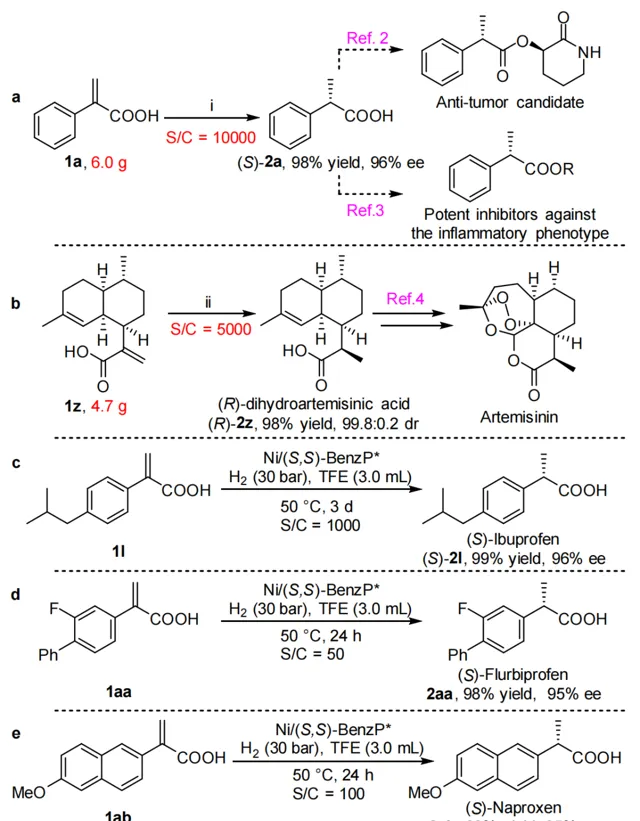
圖3 克級規模反應及套用研究
進一步地,他們對反應進行克級規模放大,發現標準受質可以在轉化數為10000的條件下獲得目標產物(圖3a)。同時,在青蒿素的重要前體(
R
)-雙氫青蒿素的獲取中,該反應也可以達到5000的轉化數,以及99.8:0.2的非對映體過量(圖3b)。另外,該方法也可以直接套用於一系列非類固醇消炎藥如(S
)-布洛芬,(S
)-氟比洛芬,(S
)-萘普生的綠色合成中。為了闡明反應的發生過程,他們借助了DFT計算,結果表明,中間體3(IM-3)經由過渡態2(TS-2)的過程中,分子內羧基質子轉移步驟是反應的動力學決速步驟和立體選擇性決定步驟(圖4)。另外,反應級數實驗表明,該反應對於受質和鎳鹽的級數是一級,對於氫氣的級數則是零級,經過動力學方程式推導,與理論計算一致。此外,透過外加酸,堿,以及使用相應的羧酸酯受質的控制實驗表明反應中的質子對於反應的活性起著至關重要的作用,這也與DFT計算的結果保持一致。
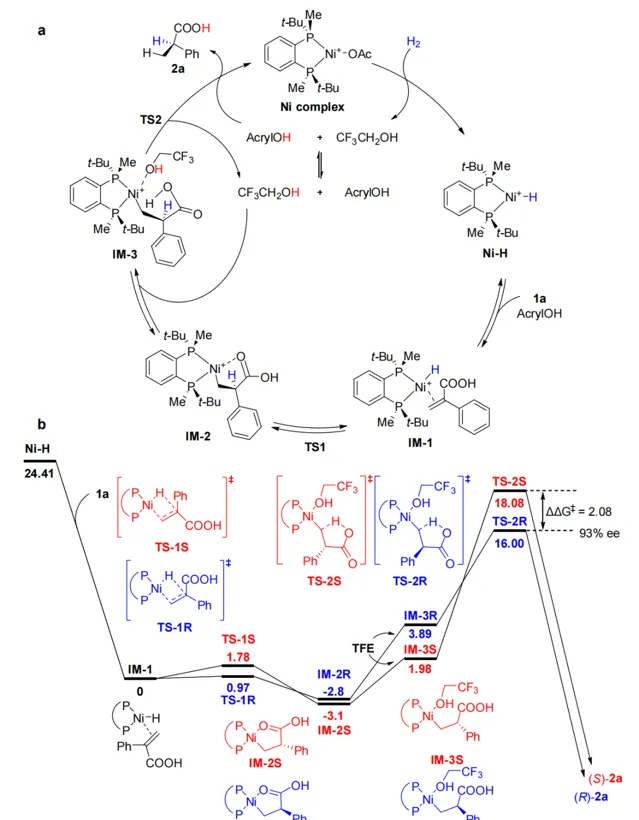
圖4 機理研究
隨後,他們借助IGMH分析視覺化的TS-2R和TS-2S構象中受質和催化劑之間的弱交互作用,發現C-H···H-C和C-H···O交互作用在兩種過渡態中都存在,但TS-2R中的交互作用明顯強於TS-2S,這表示受質和催化劑的弱交互作用可能會有助於穩定反應的過渡態和提升反應的立體選擇性。
總結
張萬斌教授課題組開發了一種高效的豐產金屬鎳催化不對稱氫化α-烷基或芳基取代的丙烯酸的方法。以優異的結果得到了相應的手性α-取代丙酸 (產率高達99%,對映選擇性高達99.4%,轉化數高達10000 S/C)。特別是在青蒿素的關鍵中間體 (
R
)-二氫青蒿酸合成中,其轉化數達到5000,且非對映體過量達到了99.8:0.2。機理研究表明,受質的羧酸基團的分子內質子轉移促使C-Ni鍵的解離是速率決定步驟。文獻詳情:
B. Li,+ Z. Wang,+ Y. Luo, H. Wei, J. Chen,* D. Liu, W. Zhang,* Nickel-catalyzed asymmetric hydrogenation for the preparation of α-substituted propionic acids.
Nat. Commun.
15, 5482 (2024). https://doi.org/10.1038/s41467-024-49801-0










