KRAS是人類最常見的致癌突變之一,尤其是在胰腺導管腺癌(PDAC)、非小細胞肺癌(NSCLC)和結直腸癌(CRC)中。作為靶向治療中的「釘子戶」一般的存在,近40年來,幾乎所有靶向藥都在KRAS基因突變的面前紛紛折戟。
2024年8月21日,中國國家藥監局(NMPA)官網公示, 達伯特®(氟澤雷塞片;信達研發代號:IBI351;勁方研發代號:GFH925) 已獲中國國家藥品監督管理局藥品審評中心批準上市,用於 至少接受過一種系統性治療的鼠類肉瘤病毒癌基因G12C(KRAS G12C)突變型的晚期非小細胞肺癌(NSCLC)成人患者。達伯特®(氟澤雷塞片)是中國首個獲批的KRASG12C抑制劑, 將惠及更多中國KRASG12C突變型的肺癌患者。

此前,2023年11月24日,中國國家藥品監督管理局已經正式受理IBI-351(KRAS G12C抑制劑)的新藥上市特許申請並納入優先審評程式。
近50%肺癌患者腫瘤消失或縮小!國內首個KRAS抑制劑達伯特獲批上市!
達伯特®(氟澤雷塞片) 是一款國研的新型、具有口服活性的強效KRAS G12C抑制劑,透過阻斷KRAS依賴的訊息傳遞,抑制腫瘤細胞的增殖,並誘導細胞雕亡。
此前, 該獲批藥物於2023年1月被CDE納入突破性治療品種 ,擬用於治療至少接受過一種系統性治療的KRAS G12C突變型的晚期非小細胞肺癌(NSCLC)患者。
此次新藥上市是基於一項在中國開展的臨床II期單臂註冊研究結果。數據截至2023年12月13日,共納入116例非小細胞肺癌患者,中位隨訪時間為15.1個月。

數據顯示,獨立影像學評審委員會(IRRC)評估的 確認的客觀緩解率(ORR)達49.1%;疾病控制率(DCR)達90.5%。
中位緩解持續時間(DoR)未達到, 12個月DoR率為53.7% 。中位無進展生存期(mPFS)9.7個月, 12個月PFS率為37.9% ;中位生存期(OS)尚未達到, 12個月OS率為54.4% 。
亞組分析顯示,各亞組在IBI351單藥治療中基本取得一致獲益,包括預後較差的腦轉移患者。 35例(30.2%)基線腦轉移患者經IRRC確認的ORR為48.6%,DCR為94.3%;81例基線無腦轉移患者經IRRC確認的ORR為49.4%,DCR為88.9%, 兩者腫瘤應答狀況相似。
基線無腦轉移患者的mPFS和mOS分別為10.4個月、14.1個月,均優於腦轉移患者的6.4個月和10.9個月。此外,氟澤雷塞顱內ORR為22.6%,顱內DCR達 96.8%,且 所有顱內緩解患者均為完全緩解(CR) 。
總而言之,IBI351單藥治療在既往經治的KRAS G12C突變晚期非小細胞肺癌中具有優異的療效和良好的耐受性。
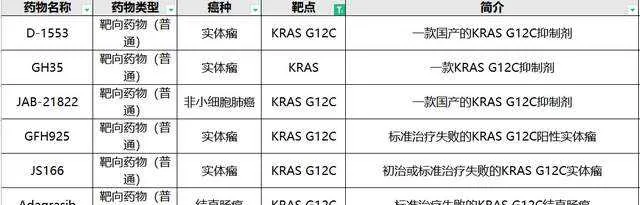
目前無癌家園有多款針對KRAS G12C的靶向藥正在臨床研究中!
詳情請戳:官宣!近50%的肺癌患者腫瘤消失或大幅縮小!國內首個KRAS抑制劑達伯特獲批上市!
靶病竈縮小100%!IBI351聯合西妥昔單抗挑戰一線治療肺癌!
Fulzerasib(IBI351)是一種KRAS G12C創新小分子抑制劑,在以往治療過的非小細胞肺癌患者的單藥治療中,已表現出顯著的治療效果。表皮生長因子受體 (EGFR) 的啟用被認為是 KRAS 抑制耐藥的主要機制之一。臨床前證據表明,在 KRAS G12C 突變 NSCLC 模型中使用Fulzerasib(IBI351)與西妥昔單抗具有協同作用。
因此,在2024年ASCO大會上,中國的研究學者們公布了關於兩者聯合一線治療KRAS G12C非小細胞肺癌的II期臨床研究結果,這也是全球首個KRAS G12C抑制劑聯合EGFR抑制劑用於一線NSCLC治療的臨床數據在國際學術會議公布。
截至2024年4月19日,共納入40例NSCLC患者,其中33例接受過至少一次治療後腫瘤評估: 客觀緩解率(ORR)為81.8%,疾病控制率(DCR)高達100%;多數可評估患者(27/33)達到腫瘤緩解,其中1例達到完全緩解,另外2例達到部份緩解的患者也觀察到靶病竈縮小100%。 此外, 這項聯合療法具有良好可控的安全性及耐受性。
疾病控制率90%!國內首個KRAS抑制劑達伯特宣戰結直腸癌!
除了非小細胞肺癌外,2023年5月,GFH925(IBI351)還被納入突破性療法,用於治療至少接受過一種系統性治療的KRAS G12C突變型的晚期結直腸癌患者。
截止到2023年6月13日,共有56例轉移性結直腸癌患者被納入分析(其中700mg QD 3名受試者,450mg BID 4名受試者,600mg BID 48名受試者和750mg BID 1名受試者) 。
結果顯示:600mg BID劑量組中共有48例受試者接受了至少一次腫瘤評估, 確認的客觀緩解率(cORR)為45.8%,疾病控制率(DCR)為89.6%。 其中共有27例受試者既往接受了2線及以上的系統性治療,確認的ORR為63.0%,DCR為88.9%。
尚未達到中位緩解持續時間 (DoR),6個月DoR率為65.5%。中位PFS為7.6個月。尚未達到中位OS,6個月OS率為91.1%。安全性方面,截至數據分析日,總體耐受性良好。
初步數據顯示IBI351單藥在KRASG12C突變的晚期結直腸癌患者中展示出了良好的安全性和令人鼓舞的療效。 我們期待該研究有更多的積極持續的結果更新。
國產抗癌藥向最難靶點宣戰!創新KRAS G12C抑制劑獲批臨床!
其實,在醫學研究者們不斷地努力之下,KRAS這座堡壘終於破防,多款新藥不斷湧現,並已有多個在研藥物在臨床研究階段取得了早期成功:包括:D-1553、JNJ-74699157 (ARS-3248)、JAB-3312、LY3499446以及泛KRAS抑制劑BI 1701963等。
1 首戰告捷!國產抗癌藥JAB-21822客觀緩解率高達70%!
2022年12月16日,加科思釋出公告稱, 公司自主研發的KRAS G12C抑制劑JAB-21822獲得國家藥監局藥品審評中心授予突破性治療藥物認定 , 用於治療KRAS G12C突變的晚期或轉移性非小細胞肺癌(NSCLC)患者。 此次認定是基於JAB-21822前期良好的療效和安全特性。


JAB-21822是加科思自主研發的KRAS G12C抑制劑。臨床前研究數據表明,其可單獨使用,治療含KRAS G12C突變的實體瘤,同時在KRAS G12C抑制劑治療發生耐藥後,聯合SHP2抑制劑有望有效克服和逆轉KRAS抑制劑的耐藥問題。

在2022年ASCO大會上,加科思公布的1期臨床數據顯示,截至2022年4月1日共入組72例晚期實體瘤患者。其中有療效評估的KRAS G12C突變的非小細胞肺癌患者共32例, 客觀緩解率(ORR)為56.3%(18/32),疾病控制率(DCR)為90.6%(29/32)。 在400mg/d及800mg/d的劑量組中, 客觀緩解率為66.7%(8/12),疾病控制率為100%(12/12)。 此外,JAB-21822在劑量遞增階段無劑量限制性毒性(DLT),400mg/d及800mg/d劑量組中三級或四級治療相關不良反應為2.5%(1/40)。
在KRAS G12C突變的實體瘤患者中,JAB-21822有良好的耐受性,並且具有顯著有效性。
2 疾病控制率85.7%,國產靶向藥D-1553首次亮相AACR!
D-1553是由益方生物自主開發的一款新型、高效且口服的KRAS G12C抑制劑。在2022年美國腫瘤研究協會(AACR)年會上,益方生物首次公布了其口服KRAS G12C抑制劑D-1553在癌癥患者中的臨床I期數據,這使得 D-1553成為了首個公布臨床數據的國產KRAS抑制劑。
在一項針對攜帶 KRAS G12C突變的晚期或轉移性實體瘤患者 的國際多中心一期研究中 , D-1553在22例患者中耐受性良好 ,沒有任何劑量限制性毒性。在21例可評估的患者中,觀察到 19.0%確認的腫瘤客觀緩解率 ,達到了 85.7%的疾病控制率 。在劑量水平低至每天300mg時已觀察到腫瘤緩解。
在另一項由上海胸科醫院陸舜教授為主要研究者,針對 攜帶KRAS G12C突變的非小細胞肺癌(NSCLC)患者 的研究分析中包括了59例患者,其中52例為可評估患者, 腫瘤客觀緩解率達到40.4%,疾病控制率高達90.4%。 這些患者均為 晚期或轉移性癌癥患者,大多數已經接受了二線或二線以上的系統性抗癌藥物治療。
數據顯示,在PR2D(600mg/BID,BID為一日兩次)劑量下, D-1553在32例患者中評估的客觀緩解率達到40.6%,疾病控制率為84.4%。 安全性方面,D-1553耐受性良好,未達到劑量限制性毒性。
據悉,D-1553已於2020年10月獲得美國FDA批準在美國、澳洲、中國台灣、南韓等國家和地區啟動了國際多中心I/II期臨床試驗,目前進展順利。並於2021年1月獲得中國國家藥品監督管理局藥品審評中心批準開展 I/II 期臨床試驗。
3 君實生物的KRAS抑制劑JS116首次在國內申請臨床
2022年3月28日,中國國家藥品監督管理局藥品審評中心(CDE)官網顯示,君實生物的KRAS抑制劑JS116首次在國內申請臨床。JS116為具有全新結構的KRASG12C小分子不可逆共價抑制劑,用於治療 KRASG12C 突變的非小細胞性肺癌(NSCLC)患者。

KRAS基因突變有不同的亞型,其中KRASG12C占所有KRAS突變的44%,在NSCLC中最為常見。臨床前研究表明,JS116具有較寬的安全窗,良好的有效性和安全性,有望成為安全、高效的精準靶向治療藥物。這也是君實在國內申報的第7款化藥新藥。
小編有話說
此外,有研究表明,KRAS G12C靶向藥與其他免疫藥、靶向藥的聯用效果會更佳!此次研究也證實聯合用藥或特許以讓更多的癌癥患者從中獲益。小編也相信,在未來將會有眾多KRAS靶向藥不斷湧現,讓更多患者有藥用,用好藥!
本文為無癌家園原創










