
撰文丨王聰
編輯丨王多魚
題圖丨Pixabay
近年來,微生物組研究揭示了體內的共生細菌表達的基因透過多種機制影響我們的健康。例如,體內的細菌還能夠影響癌癥免疫療法的效果;細菌蛋白質與神經退行性疾病和自身免疫性疾病有關;細菌毒素能夠引發包括癌癥在內的一系列急性和慢性疾病;細菌能夠改變或隔離藥物,影響治療效果。這些研究和發現激發了人們對操縱微生物組的興趣,這既為了更好地理解它們,也為了開發新療法。
基於CRISPR的基因編輯工具在編輯人類細胞中的致病基因方面取得了巨大成功,但我們目前缺乏在體內原位細菌(例如腸道菌群)上取得類似成功的工具。
2024年7月10日,基因編輯公司Eligo Bioscience的研究人員在國際頂尖學術期刊Nature上發表了題為:In situ targeted base editing of bacteria in the mouse gut 的研究論文。
該研究開發了工程改造的λ噬菌體,利用噬菌體誘導染色體島(phage-inducible chromosomal island,PICI)復制機制的DNA有效載荷,遞送堿基編輯器,首次實作了在活體小鼠體內對腸道細菌的高效、精準基因編輯,且能夠避免遞送進體內的DNA有效載荷的復制和傳播。
該研究開發的堿基編輯系統代表了體內原位編輯細菌的工具的關鍵性飛躍,開啟了編輯微生物以對抗疾病的可能性。

在這項最新研究中,研究團隊提出了一種對目標腸道菌群進行原位、精確且穩定的基因修飾策略。
要想在復雜的腸道環境中實作這一目標,需要高效的DNA遞送與有效的靶向誘變策略相結合。研究團隊探索了將噬菌體來源的顆粒(phage-derived particles)用作遞送載體,並與堿基編輯器(base editor)相結合。堿基編輯器能夠在不產生DNA雙鏈斷裂的情況下,在目標位點將一個堿基對轉換為另一個堿基對,並且已在包括廣泛的細菌物種在內的各種生物中成功套用。
此前已有多項研究探索了向目標細菌遞送CRISPR - Cas系統,這些研究使用了多種遞送模式,包括供體細菌的質體與目標菌株的結合、包裝到噬菌體衣殼中的質體的轉導,或者將CRISPR-Cas系統添加到噬菌體基因組中。由於噬菌體DNA遞送效率高,它們成為一種有吸重力的載體選擇。當目標是只編輯而不殺死細菌時,就不能使用裂解性噬菌體,而是使用噬菌粒或溫和噬菌體。
此前向小鼠腸道中大腸桿菌進行DNA遞送的研究,要麽依賴於M13噬菌粒,要麽依賴於基因修飾的λ噬菌體。M13噬菌粒以F菌毛作為受體,這限制了其範圍,並且M13在透過小鼠胃腸道時不穩定。而λ噬菌體,在感染大腸桿菌時,λ要麽進入裂解周期並產生更多的病毒顆粒,要麽進入溶原化並整合到染色體中(從而能夠維持遞送的諸如I型 CRISPR–Cas系統或dCas9等轉基因)。最近還有研究在λ噬菌體基因組中引入了堿基編輯器,盡管其能夠在腸道環境中繁殖,但λ噬菌體無法使整個目標群體溶原化。
為了提高腸道環境中的遞送效率,研究團隊設計了λ噬菌體尾部的多個嵌合變體以靶向不同的受體。
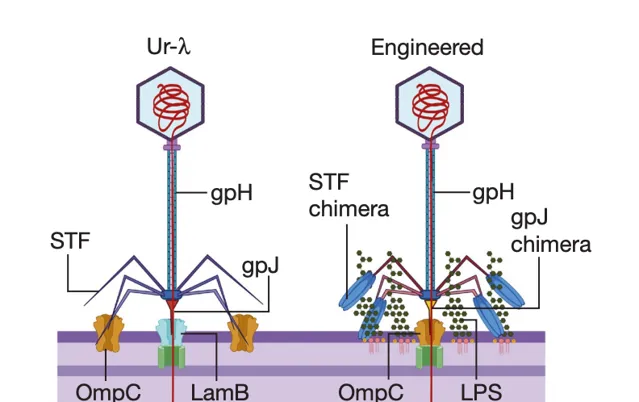
原位靶向誘變策略的另一個理想特征是它不會進一步傳播遞送進去的轉基因。為實作這一目標,研究團隊開發了一種利用噬菌體誘導染色體島(phage-inducible chromosomal island,PICI)復制機制的DNA有效載荷。這一設計能夠確保所遞送的DNA在受體細菌中不會復制,同時仍能有效表達堿基編輯器。這種策略能夠在無需選擇壓力或維持轉基因的情況下,為定植在小鼠腸道中的大多數大腸桿菌群體引入穩定的遺傳擾動。
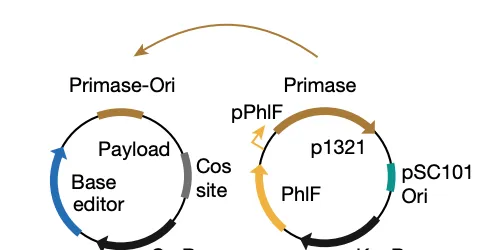
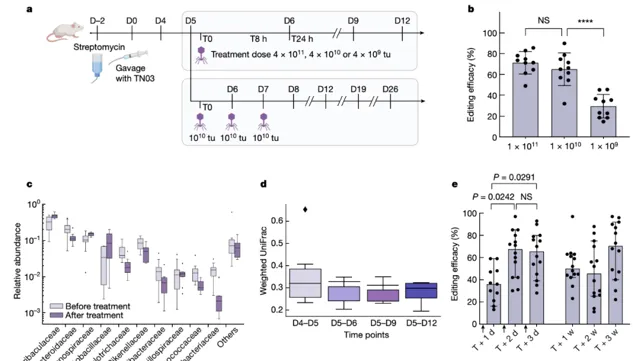
具體來說,該研究設計了一種噬菌體來源的顆粒,用於遞送堿基編輯器,並對定植於小鼠腸道中的大腸桿菌的β-內醯胺酶基因(該酶能夠水解青黴素等抗生素,幫助細菌抵抗抗生素)進行基因編輯。實驗結果顯示,單次編輯使目標細菌群體的中位編輯效率達到93%,編輯後的大腸桿菌在小鼠腸道中穩定維持至少42天。此外,由於該研究使用了非復制型DNA載體,防止了有效載荷的維持和傳播。
然後,研究團隊利用這種方法在體外成功對大腸桿菌和肺炎克雷伯菌菌株中的幾個治療相關基因進行堿基編輯,並證明了該方法可在體內原位編輯致病性大腸桿菌參與卷曲菌毛(curli,其與多種神經退行性疾病和自身免疫病相關)產生的基因,編輯效率約為70%。
總的來說,這項研究證明了直接在活體動物腸道中對細菌進行精準基因編輯的可行性,為研究細菌基因的功能提供了新途徑,並為設計新的微生物組靶向療法開啟了大門 。
研究團隊表示,下一步將開發具有微生物組驅動疾病的小鼠模型,用於評估對這些微生物的基因編輯是否有有益影響。
論文連結:











