油和水不能互溶,僅限於純水和純油不能互溶,但是如果包含有其他的物質的話,情況就不一定了。
比如碗中的油漬,一般我們是如何洗掉的呢?加洗潔精。為什麽加了洗潔精後,就很容易洗掉油漬了呢?那是因為洗潔精中有類叫做表面活性劑的物質,將油漬「加溶」到了水中。
什麽是表面活性劑:
表面活性劑通常是一類具有兩親性的分子。所謂兩親性,指的是同時具有親水性和親油性。親水性是指的極性基團,容易與水分子形成氫鍵,比如羥基或者具有電荷;親油性是指的非極性基團,憎水,比如CH鏈。
而在表面活性劑中,一般一端是親水的,一端是親油的。比如在下圖中的十二烷基硫酸鈉(SDS)中,左端就是親油端(有些地方叫做疏水端),右端就是親水端。
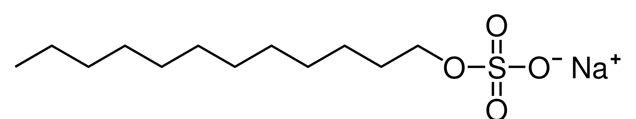
當僅有極少量的表面活性劑在水中時,它們會富集在水溶液的表面——因為表面活性劑中的親油基團傾向於遠離水。這時候,它們會在水溶液表面,並且親水端在水中,而親油端指向空氣。
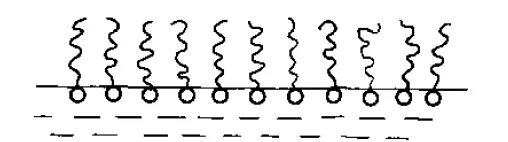
而當表面活性劑達到一定的濃度CMC時(CMC:臨界膠束濃度),表面活性劑會在水中形成分子有序結構。這是因為此時水溶液表面已經全被占據,必須有一些表面活性劑在水中;但是另一方面,依然要保證疏水端遠離水。所以這時候就會形成膠束之類的結構。
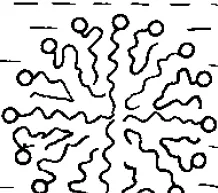
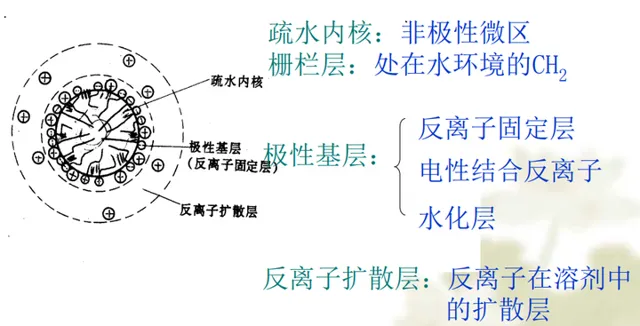
那麽此時,由於水溶液中這些膠束的存在,實際上水中存在一些親油的位點的!就是這些膠束的中心——疏水內核。那麽,一些有機分子,比如油,在具有膠束的溶液中溶解度將會大幅增加!這就是表面活性劑的加溶作用。比如2-硝基二苯胺在水中難溶,但是在月桂酸鉀(一種表面活性劑)溶液中,當達到CMC後溶解度飆升。
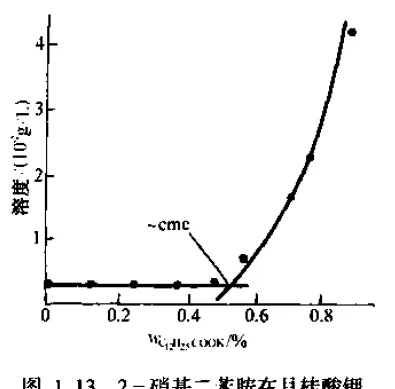
小結:油水不能互溶,只是純油和純水不能互溶。但是,如果還有表面活性劑存在,並且達到了一定的濃度(CMC),那麽油是可以被加溶到水中的。
那麽,湯中是否存在這樣的表面活性劑呢?
在熬湯的過程中,食材中的蛋白質和磷脂會逐漸被煮出來。蛋白質和磷脂,都是同時具有親水基團和疏水基團的物質,所以它們是可以充當表面活性劑的作用的。
總結:在熬湯的過程中,由於食材中的蛋白質和磷脂溶入水中充當了表面活性劑的角色,使得油得以被加溶。
最後推薦幾個閱讀材料:
首先是技術型吃貨錢程大V的文章。註意在食品科學中,一般用「乳化劑」這個稱謂代替「表面活性劑」。
其次是趙國璽老師的【表面活性劑作用原理】一書。這是一本非常經典的界面化學領域的教材。

然後是北京大學黃建濱老師的界面化學課件
還有該經典教材,不過我暫時還沒有讀過











